抑郁症(major depressive disorder,MDD)的经典理论强调慢性应激导致5-HT/DA/MT等单胺能递质功能低下。但一个长期被低估的线索是:外源性甲醛(formaldehyde,FA)暴露可诱发抑郁样症状。而应激是否会驱动内源性FA升高,并成为抑郁触发因素尚不清楚。

该研究采用细胞-小鼠-人群的递进策略,开展跨尺度、跨物种的系统研究。细胞层面:用FA荧光探针定位FA来源与诱发条件,检验谷氨酸超兴奋与线粒体代谢的关系;动物层面:急/慢性应激(含CUMS)定量小鼠海马CA1 FA变化;通过海马CA1局部FA显微注射与腹腔慢性FA注射直接验证FA与抑郁之间的因果联系;用膜片钳记录CA1放电/兴奋性及突触功能;并以质谱证明FA对单胺的化学“失活”;人群层面:模拟失重应激(Head-down Tilt,HDT)追踪情绪量表与尿FA动态;ENIGMA数据库青少年MDD海马分区定量,强调CA1萎缩;并在MDD患者血清中检测FA代谢相关酶、FA并与HAMD评分等临床量表进行关联。主要发现如下:
1. 神经超兴奋触发FA生成:线粒体SARDH是关键节点
细胞层面,谷氨酸(Glu)诱导的细胞超兴奋使线粒体靶向FA信号显著升高,并伴随SARDH活性增强;钙螯合与线粒体通透性转换孔阻断剂CysA,可抑制这一过程,提示FA生成与Ca²⁺依赖的线粒体代谢耦联。
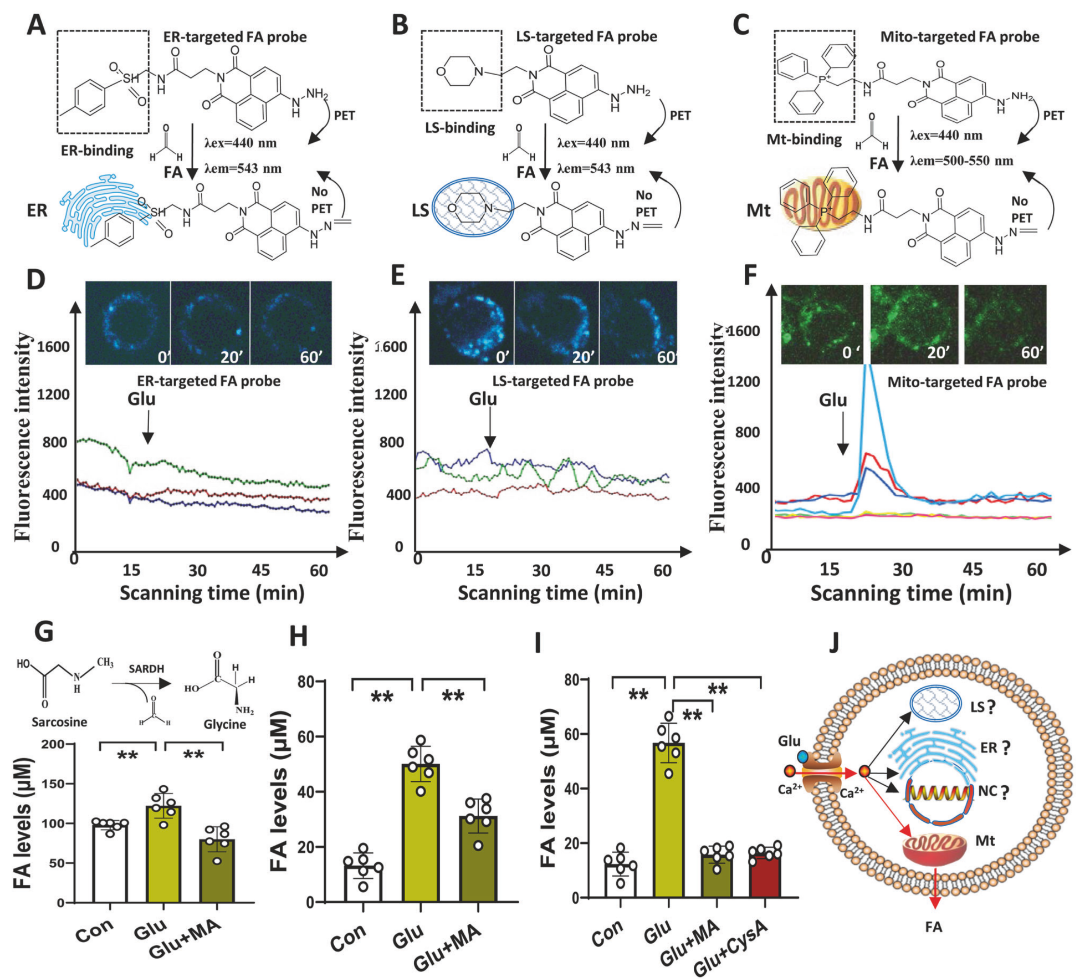
图1:兴奋性神经递质谷氨酸会促使线粒体中产生活性FA。
2. 急性与慢性应激均使海马CA1 FA积累:并伴随FA生成酶上调
多种急性应激可快速提升海马CA1 FA荧光信号;在CUMS模型中,FA生成相关酶(如SSAO、SARDH)水平升高,提示慢性应激可造成更持久的FA积累。
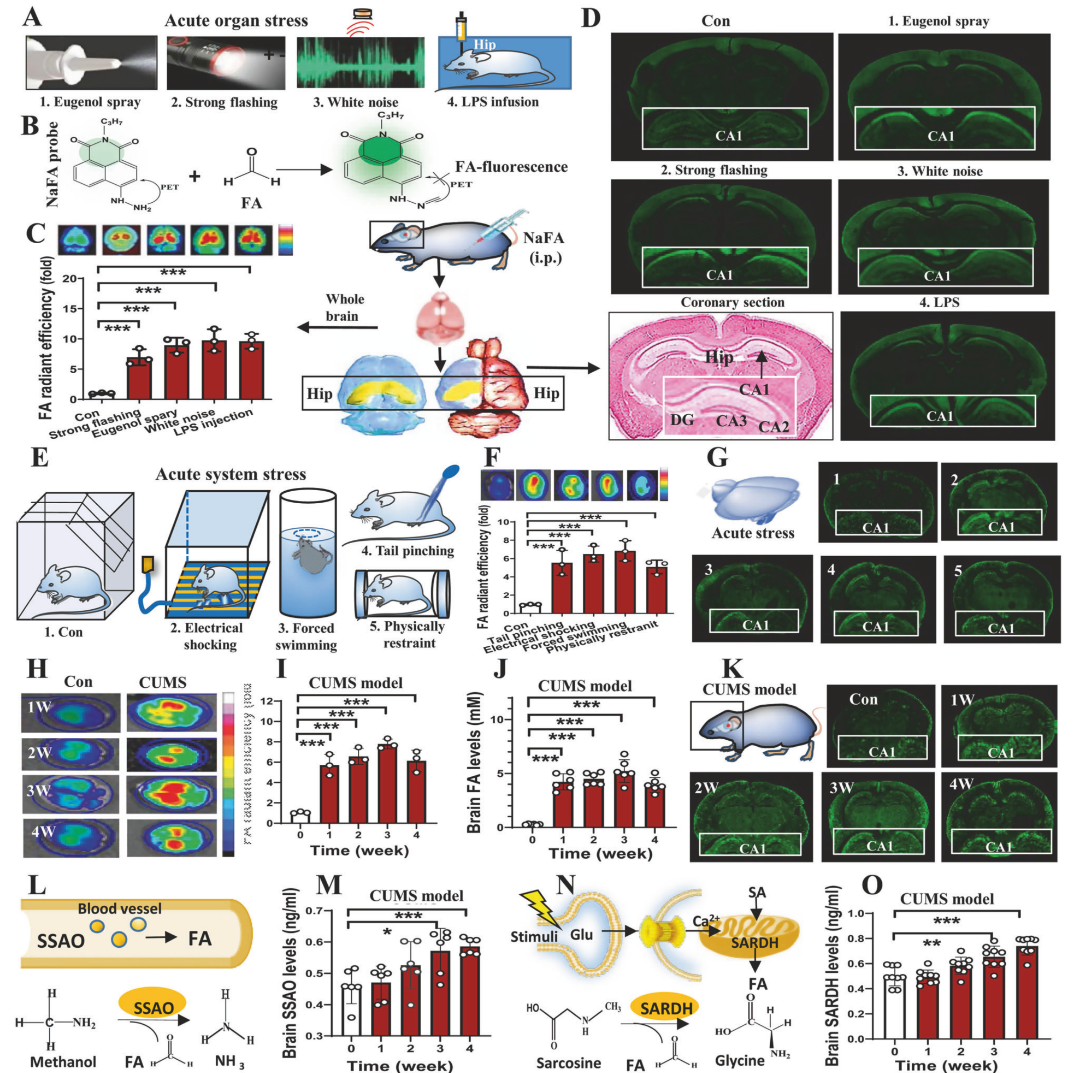
图2:在野生型小鼠经历急性器官和急性系统应激后,海马体CA1区产生FA。
3. FA不止与抑郁“相关”,更有“致病因果性”:体内FA过量可诱发抑郁样行为
提高CA1局部或全身FA可直接诱发抑郁样行为,并伴随单胺下降与CA1损伤。对小鼠双侧CA1连续14天注射FA可显著增加TST/FST不动时间、降低糖水偏好,同时海马5-HT/DA/MT下降;腹腔慢性注射FA同样导致抑郁样行为,并在较高水平下出现海马CA1神经元损伤。
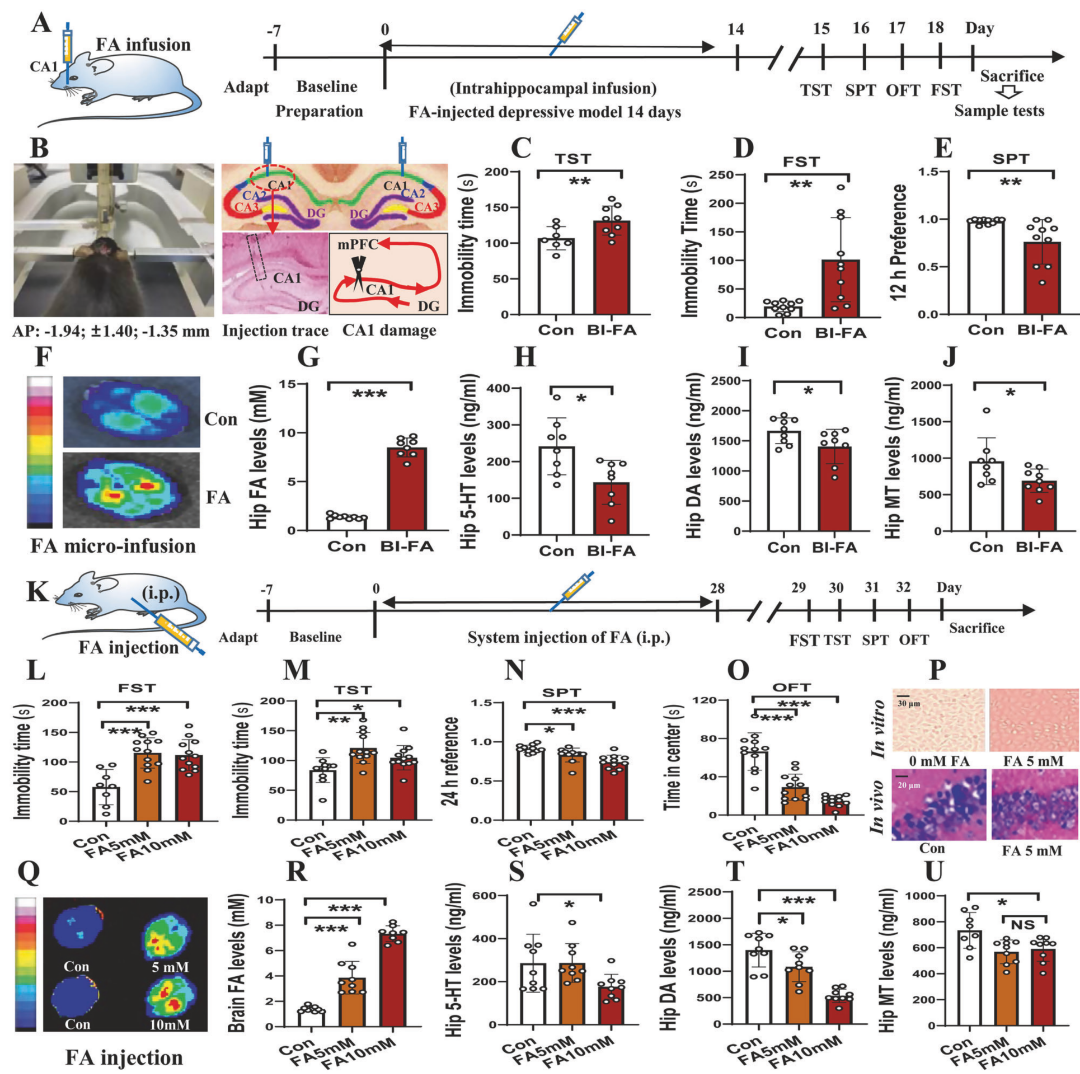 图3:无论是急性还是慢性注射FA,都会导致小鼠出现抑郁样行为。
图3:无论是急性还是慢性注射FA,都会导致小鼠出现抑郁样行为。
4. 机制核心:FA与单胺发生化学反应,导致“单胺失活/耗竭”,同时损害CA1功能
慢性应激导致抑郁样行为并伴随单胺类递质减少。将FA与5-HT、DA、MT在生理条件下共同孵育,观察到FA水平下降并生成反应衍生物(GC–MS/MS),且ELISA测得单胺浓度显著降低,支持FA可通过化学反应直接“失活”单胺,为“单胺不足”提供了一个非经典的化学耗竭路径。在电生理层面,FA对CA1自发放电/兴奋性呈剂量依赖性;较低浓度可洗脱并恢复,而更高浓度FA可造成不可逆损害。与此同时,FA负荷与CA1神经元损伤相一致,提示其不仅影响递质浓度,也直接抑制CA1突触传递。
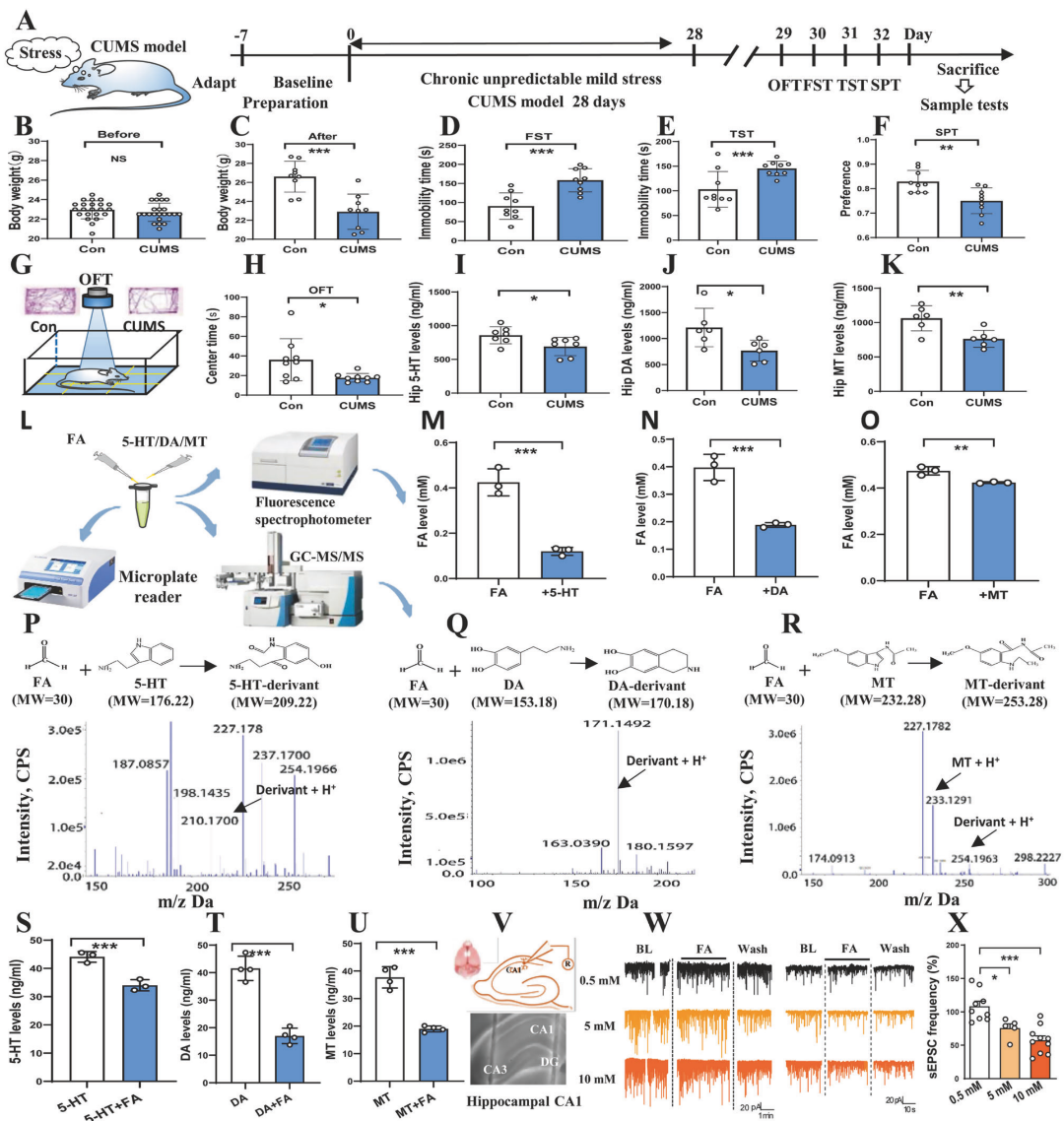 图4:在CUMS模型小鼠的海马体中,FA水平、单胺类物质水平以及神经元兴奋性的变化情况。
图4:在CUMS模型小鼠的海马体中,FA水平、单胺类物质水平以及神经元兴奋性的变化情况。
5. 临床一致性:MDD的CA1萎缩,血FA与抑郁指标相关
模拟失重应激追踪海马功能、情绪量表与尿FA动态变化,发现连续20天模拟失重导致海马过度激活,并伴随抑郁样情绪及尿液FA含量增加。在ENIGMA青少年样本中,海马总体积下降,其中CA1亚区萎缩更为突出。
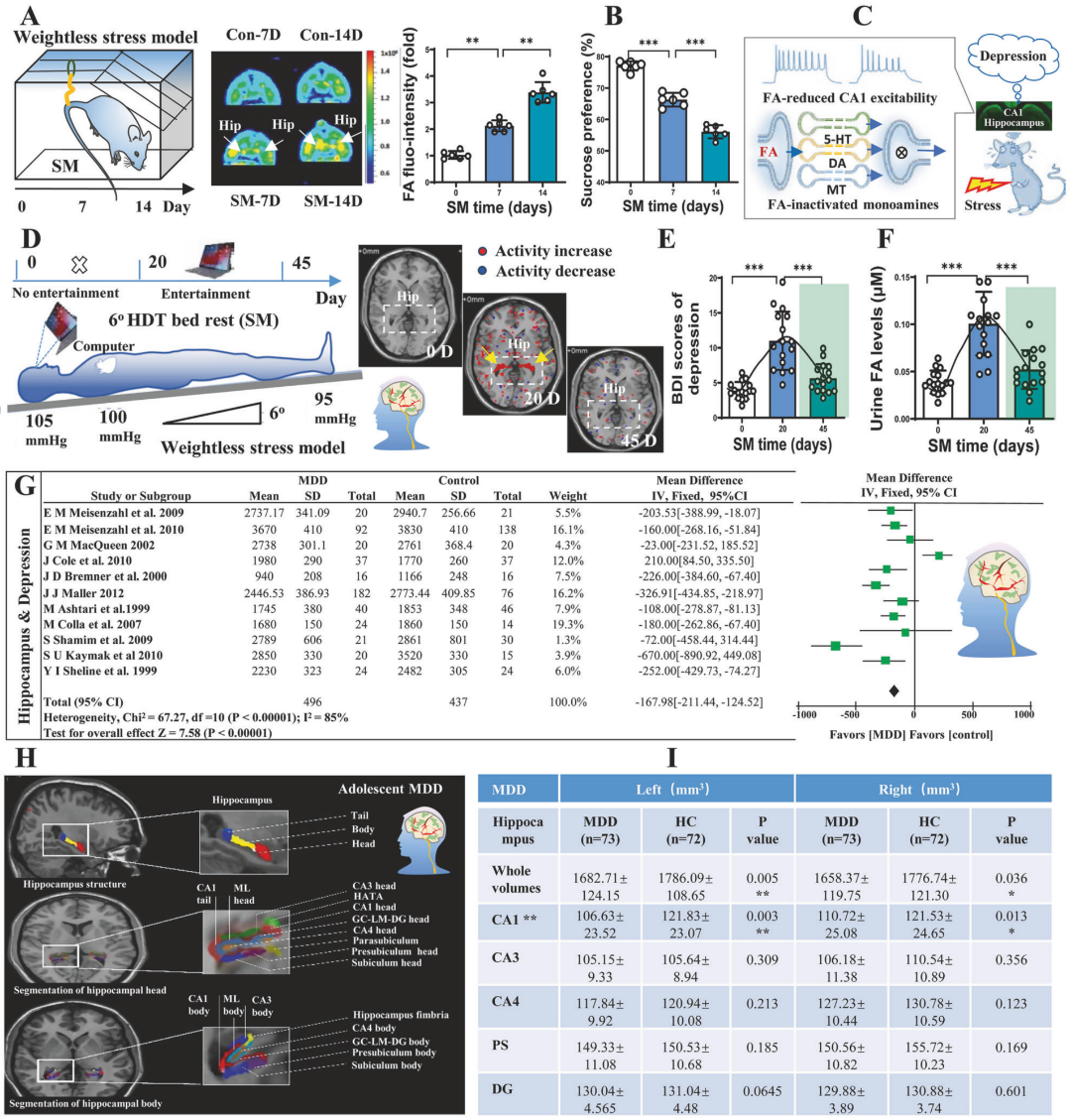 图5:青少年抑郁症患者中应激调控抑郁和导致海马体CA1区受损。
图5:青少年抑郁症患者中应激调控抑郁和导致海马体CA1区受损。
在MDD患者队列中,血清SSAO/SARDH水平与活性均升高、FDH相关指标下降,血清FA升高,同时5-HT/DA/MT下降。FA与HAMD评分正相关,FDH与FA或抑郁评分负相关。形成“FA负荷-单胺不足-抑郁症状严重度”的可量化链条。
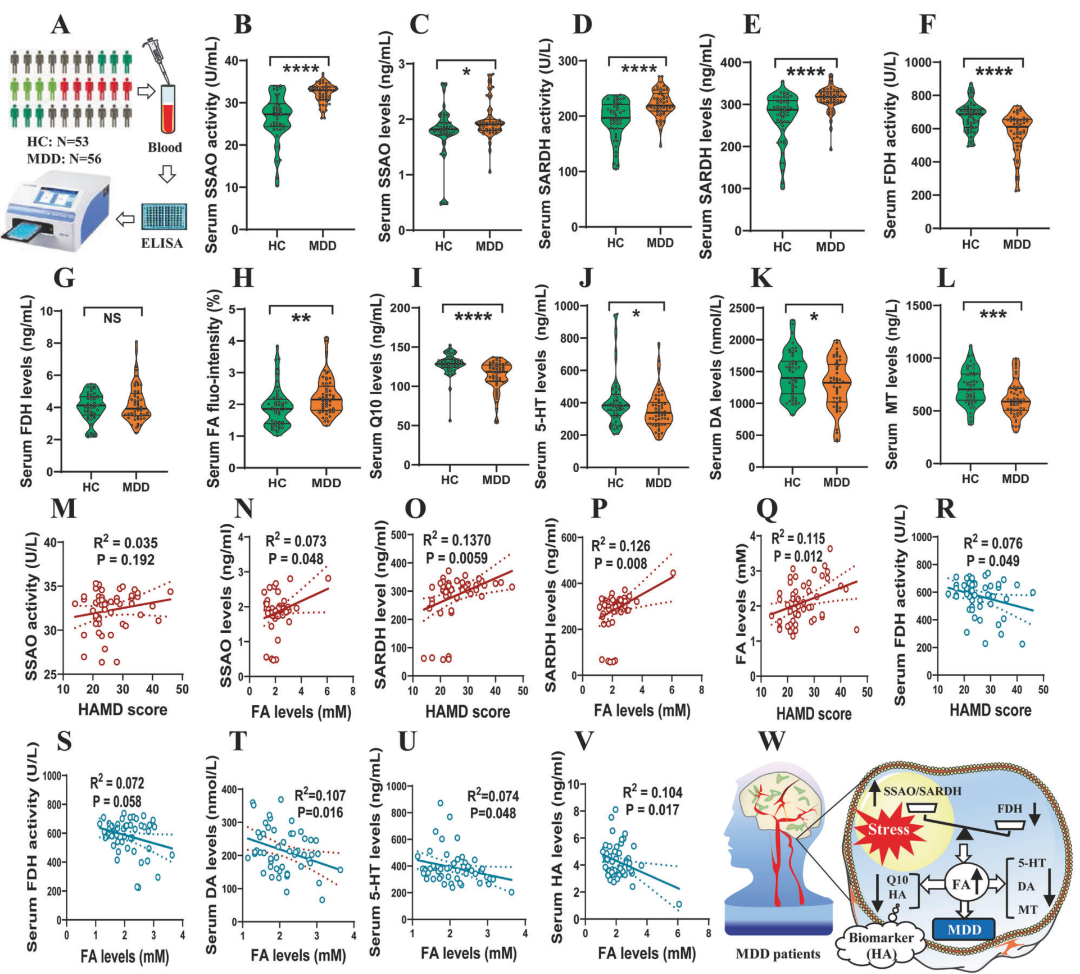 图6:青少年抑郁症患者中出现FA代谢紊乱和FA积累。
图6:青少年抑郁症患者中出现FA代谢紊乱和FA积累。
文章结论与讨论,(未来)启发与展望
该研究以“应激-海马-单胺缺乏”为主线,提出应激不仅通过经典的HPA轴影响情绪,还可驱动内源性FA在海马CA1区生成并累积,进而失活5-HT、DA与MT并抑制CA1神经元兴奋性,最终导致抑郁样表型。该工作将一个常被视为“外源毒物”的小分子FA,重新定位为应激相关的内源性关键分子,并给出了从细胞、动物到人群与影像学的跨尺度证据。
该文用FA这一关键分子将应激损伤海马、单胺缺失有效连接。串成了具有因果指向的链条:兴奋性驱动(Glu/Ca²⁺)→线粒体FA生成(SARDH等)→单胺化学失活+CA1兴奋性下降→结构性损伤/萎缩→抑郁表型与严重程度。更重要的是,在动物模型基础上,进一步结合脑体积与临床生化相关指标把“CA1-FA-单胺”框架推向人群层面。
本研究提示外周血FA及其代谢酶(SSAO/SARDH/FDH)有望用于抑郁严重度及预后评估。同时提出“清除/捕获FA”可能成为MDD的治疗方向;理论上可从降低生成(抑制SSAO/SARDH)、增强降解(改善FDH功能)、提高清除(如Q10等)三个方面切入。
瓯江实验室谭涛研究员和北京老年医院童志前教授、张平教授为本文共同通讯作者;瓯江实验室硕士吴一箐、助理研究员王为,河北大学唐永和教授,武汉科技大学梅宇飞讲师为本文共同第一作者。瓯江实验室为本文第一作者单位和第一通讯作者单位。
原文链接:
https://doi.org/10.1038/s41380-025-03405-2